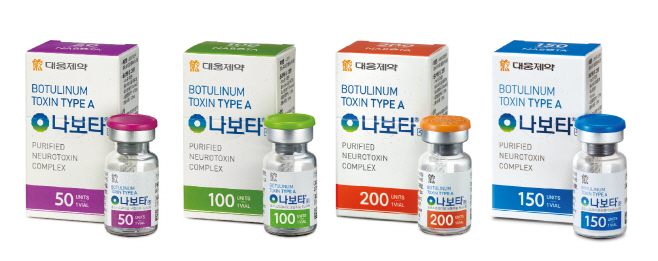
대웅제약 자체개발 보톡스 ‘나보타’, 중국서 임상 3상 본격 추진
내년 초 임상시험 마치고 NDA 제출 목표
|
대웅제약은 지난 9월 나보타의 중국 임상 3상 환자 모집을 완료하고, 임상시험을 본격 추진 중인 것으로 알려졌다. 현 추세대로라면 내년 초 임상 시험을 완료하고 신약허가(NDA) 제출이 가능할 것으로 예상된다.
대웅제약은 임상 3상을 통해 중등증~중증의 미간주름이 있는 환자 약 500명을 대상으로 16주 간 대조약과 효과를 비교, 비열등성과 제품의 안전성을 입증한다. 임상시험은 중국 내 성형 분야로 유명한 상해교통대학부속병원 제9병원을 포함한 12개 기관에서 진행 중이다.
중국 식품의약품관리총국(CFDA)에 따르면 대웅제약의 임상 3상 첫 대상자 등록은 8월 14일 이뤄졌다. 지난 9월 전체 대상자 모집이 종료돼 약 40일 만에 빠르게 환자 모집을 완료했다. 중국에서 임상 3상을 진행한 바 있는 국내 업체들의 환자 모집 기간이 6~8개월이었던 점을 감안하면 매우 빠른 속도다. 특히 신종 코로나바이러스 감염증(코로나19)의 확산 속에서 이뤄낸 결과라 더욱 의미가 있다.
중국 보툴리눔 톡신 시장은 현재 약 5000억 ~ 6000억 원 규모로, 전세계에서 미국과 유럽 다음으로 큰 규모다. 수년 간 미국 엘러간과 중국 란저우연구소의 양대 축으로 구성돼왔으나, 올해 프랑스 입센과 국내 휴젤이 새롭게 품목 허가를 획득했다.
대웅제약이 중국 시장에 성공적으로 진출하게 되면, 국내 최초로 세계 3대 보툴리눔 톡신 시장인 미국·유럽·중국에 모두 진출하는 회사가 된다. 세계 보툴리눔 톡신 시장은 약 5조원 규모로 미국·유럽·중국이 전세계 시장의 70% 이상을 차지하고 있다. 나보타의 중국 행보가 더욱 눈길을 끄는 이유다.
대웅제약은 현재 전세계 52개국에서 품목허가를 획득하고 80여개국과 수출 계약 체결을 완료했다. 현재 미국·캐나다·중남미·아시아 주요 국가에 출시됐으며, 내년에는 유럽·중동 등에 출시를 계획하고 있다.
대웅제약 관계자는 “중국은 대상 환자가 전세계에서 가장 많은 반면 시장 침투율이 2%대로 매우 낮아 미래 성장이 더욱 기대되는 시장”이라며 “나보타의 우수한 품질을 기반으로 또 하나의 거대시장인 중국으로의 진출도 차질없이 준비해 나갈 것”이라고 밝혔다.
많이 본 뉴스
연예가 핫 뉴스
오늘의 주요뉴스
- 헌재 “형제자매에 유산상속 강제하는 유류분 제도 위헌”
- 尹-李 회담 2번째 실무회동도 빈손…의제 조율 신경전
- 반도체·자동차 쌍끌이…1분기 韓 경제 1.3% ‘깜짝성장’
- 이름 바꿨다고 2억 올랐네…요지경 서울 아파트 개명
- 정부 “의료계 ‘원점 재검토·1년 유예’ 선택 불가한 대안”
- 민희진 “하이브가 날 배신했다” 경영권 찬탈 의혹 부인
- “北 무기 운송해 美제재 받은 러시아 선박, 중국에 정박”
- 생활가전 밀고 전장 끌고…LG전자, 1분기 최대매출 기록
- 외신 만난 이준석 “국민들 윤석열·이재명 외교 정책 몰라”
- 최태원, 엔비디아 젠슨 황 만나 “함께 AI 미래 만들자”






![[집파보기] 이름 바꿨다고 2억 올랐네…요지경 아파트 개..](https://img.asiatoday.co.kr/webdata/content/2024y/04m/25d/20240425010013840_77_50.jpg?c=202404260600?1)
![[집파보기] “아파트명이 곧 집값”…1%라도 올리려 ‘꼼..](https://img.asiatoday.co.kr/webdata/content/2024y/04m/25d/20240425010014423_77_50.jpg?c=202404260600?1)
![[집파보기] 라엘에스·포레온·일루미…아파트 ‘펫네임’ 열..](https://img.asiatoday.co.kr/webdata/content/2024y/04m/25d/20240425010014025_77_50.jpg?c=202404260600?1)














